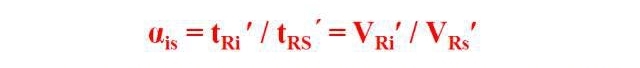cromatografia, cunoscută și sub denumirea de „analiza cromatografică”, „cromatografie”, este o metodă de separare și analiză, care are o gamă foarte largă de aplicații în chimia analitică, chimia organică, biochimie și alte domenii.
Fondatorul cromatografiei este un botanist rus M.Tsvetter.În 1906, botanistul rus Zvetter a publicat rezultatele experimentului său: Pentru a separa pigmenții de plante, a turnat extract de eter de petrol care conține pigmenți de plante într-un tub de sticlă care conținea pulbere de carbonat de calciu și l-a eluat cu eter de petrol de sus în jos.Deoarece diferiți pigmenți au capacități de adsorbție diferite pe suprafața particulelor de carbonat de calciu, odată cu procesul de leșiere, diferiți pigmenți se deplasează în jos cu viteze diferite, formând astfel benzi de culori diferite.Componentele pigmentului au fost separate.El a numit această metodă de separare cromatografie.
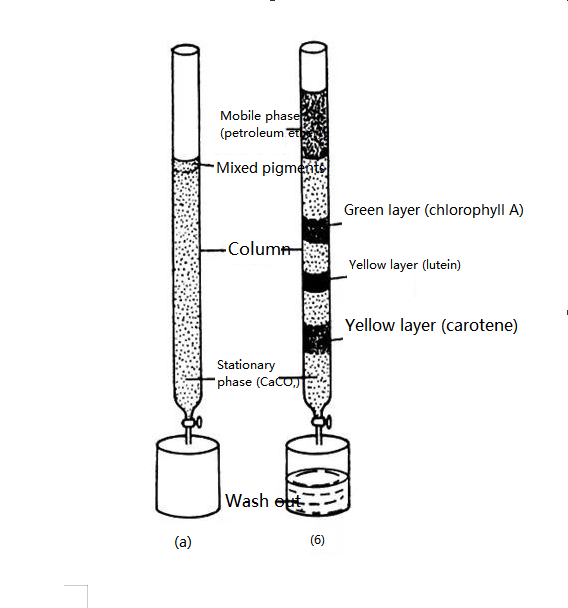
Reprezentare schematică a unui experiment de separare a pigmentului frunzelor plantei
Odată cu dezvoltarea continuă a metodelor de separare, tot mai multe substanțe incolore devin obiectul separării, cromatografia și-a pierdut treptat sensul de „culoare”, dar numele este încă în uz astăzi.
Clasificare cromatografică
Esența cromatografiei este un proces în care moleculele care trebuie separate sunt împărțite și echilibrate între faza staționară și faza mobilă.Diferite substanțe sunt împărțite diferit între cele două faze, ceea ce le face să se miște cu viteze diferite cu faza mobilă.Odată cu mișcarea fazei mobile, diferite componente din amestec sunt separate unele de altele pe faza staționară.În funcție de mecanism, acesta poate fi împărțit într-o varietate de categorii.
1, conform clasificării stării fizice în două faze
Faza mobilă: cromatografia gazoasă, cromatografia lichidă, cromatografia fluidelor supercritice
Faza staționară: gaz-solid, gaz-lichid;Lichid-solid, lichid-lichid
2, conform formei de clasificare a fazei staționare
Cromatografia pe coloană: cromatografia pe coloană compactă, cromatografia pe coloană capilară, cromatografia pe coloană micropachetă, cromatografia preparativă
Cromatografia plană: cromatografia pe hârtie, cromatografia în strat subțire, cromatografia cu membrană polimerică
3, clasificate după mecanismul de separare
Cromatografia de adsorbție: Diferitele componente sunt separate în funcție de capacitățile lor de adsorbție și desorbție pe adsorbanți
Cromatografia de partiție: Diferitele componente sunt separate în funcție de solubilitatea lor în solvent
Cromatografia de excludere moleculară: în funcție de dimensiunea dimensiunii moleculare a separării în cromatografia cu schimb de ioni: diferite componente ale afinității pentru separarea rășinii schimbătoare de ioni
Cromatografia de afinitate: Separare folosind prezența unei afinități specifice între macromoleculele biologice
Electroforeza capilară: componentele au fost separate în funcție de diferențele de mobilitate și/sau comportament de partiție
Cromatografia chirală este utilizată pentru separarea și analiza medicamentelor chirale, care pot fi împărțite în trei categorii: metoda reactivului de derivatizare chirală;Metoda aditivă a fazei mobile chirale;Metoda de rezoluție a fazei staționare chirale
Terminologie de bază pentru cromatografie
Curbele obținute prin trasarea semnalelor de răspuns ale componentelor după detectarea separării cromatografice în timp se numesc cromatograme.
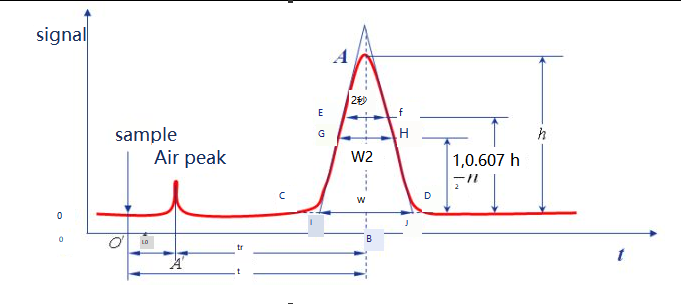
De bază:În anumite condiții cromatografice, curba semnalului generat atunci când doar faza mobilă trece prin sistemul detector se numește linia de bază, așa cum se arată în linia ot.Când condiția experimentală a fost stabilă, linia de bază a fost o linie paralelă cu axa orizontală.Linia de bază reflectă zgomotul instrumentului, în principal al detectorului, în timp.
Înălțimea vârfului:distanța verticală dintre punctul de vârf cromatografic și linia de bază, notată cu h, așa cum se arată în linia AB.
Lățimea regiunii:Lățimea regiunii vârfului cromatografic este direct legată de eficiența separării.Există trei metode pentru a descrie lățimea vârfului cromatografic: abaterea standard σ, lățimea vârfului W și FWHM W1/2.
Abaterea standard (σ):σ este jumătatea distanței dintre cele două puncte de inflexiune pe curba de distribuție normală, iar valoarea lui σ indică gradul de dispersie a componentelor departe de coloană.Cu cât valoarea lui σ este mai mare, cu atât componentele efluentului sunt mai dispersate și efectul de separare este mai rău.În schimb, componentele efluente sunt concentrate și efectul de separare este bun.
Lățimea vârfului W:Punctele de intersecție de pe ambele părți ale vârfului cromatografic sunt folosite ca linii tangente, iar interceptarea pe linia de bază se numește lățimea vârfului sau lățimea liniei de bază, care poate fi exprimată și ca W, așa cum se arată în Figura IJ.Conform principiului distribuției normale, relația dintre lățimea vârfului și abaterea standard poate fi dovedită a fi W=4σ.
W1/2:Lățimea vârfului la jumătatea înălțimii vârfului se numește FWHM, așa cum se arată pentru distanța de GH.W1/2=2,355σ, W=1,699W1/2.
W1/2, W sunt ambele derivate din σ și sunt utilizate pentru a calcula zonele de vârf în plus față de măsurarea efectului coloanei.Măsurarea FWHM este mai convenabilă și mai frecvent utilizată.
rezumat scurt
Din curba cromatografică a debitului de vârf se pot atinge următoarele obiective:
a, Analiza calitativă a fost efectuată pe baza valorii de retenție a vârfurilor cromatografice
b, analiza cantitativă bazată pe aria sau vârful vârfului cromatografic
C. Eficiența de separare a coloanei a fost evaluată în funcție de valoarea de retenție și lățimea vârfului picului cromatografic
Formula de calcul implicată în cromatografie
1. Valoarea de retenție
Valoarea de retenție este un parametru utilizat pentru a descrie gradul în care o componentă a probei este reținută în coloană și este utilizat ca indicator al caracterizării cromatografice.Metoda sa de reprezentare este următoarea:
Timp de retenție tR
Ora decesuluitM
Reglați timpul de retenție tR'=tR-tM
(Timp total petrecut în faza staționară)
Volumul de retenție
VR=tR*F.(independent de viteza fazei mobile)
Volum mort
VM=tM*Fc
(Spațiul neocupat de faza staționară în calea de curgere de la injector la detector)
Reglați volumul de retenție VR'=t'R*Fc
2. Valoarea relativă de retenție
Valoarea relativă de retenție, cunoscută și sub denumirea de factor de separare, raport al coeficientului de partiție sau factor de capacitate relativă, este raportul dintre timpul de retenție ajustat (volumul) al componentei testate și timpul de retenție ajustat (volumul) al standardului în anumite condiții cromatografice.

Valorile relative de retenție au fost utilizate pentru a elimina influența anumitor condiții de funcționare, cum ar fi debitul și pierderile de fixare, asupra valorilor de retenție.Standardul în valoarea relativă de retenție poate fi o componentă din proba testată sau un compus adăugat artificial.
3. Indicele de retenție
Indicele de retenție este indicele de retenție al substanței i care urmează să fie testată într-o soluție fixă X. Sunt selectați doi n-alani ca substanțe de referință, dintre care unul are număr de atomi de carbon N, iar celălalt are N+n.Timpul de retenție ajustat al acestora este t 'r (N) și respectiv t 'r (N+n), astfel încât timpul de retenție ajustat t 'r (i) al substanței i de testat să fie exact între ele, adică t 'r (N).
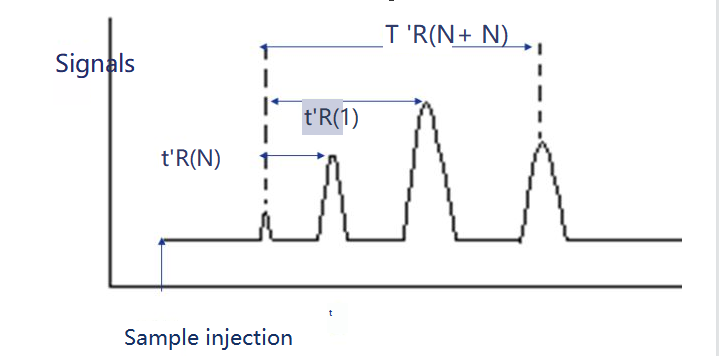
Indicele de retenție poate fi calculat după cum urmează.
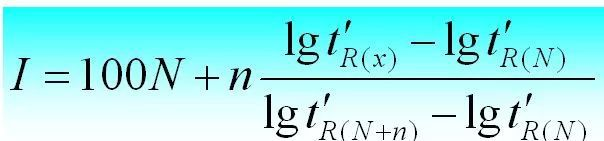
4. Factorul de capacitate (k)
La echilibru, raportul dintre masa unei componente în faza staționară (s) și faza mobilă (m), numit factor de capacitate.Formula este următoarea:
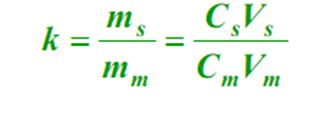
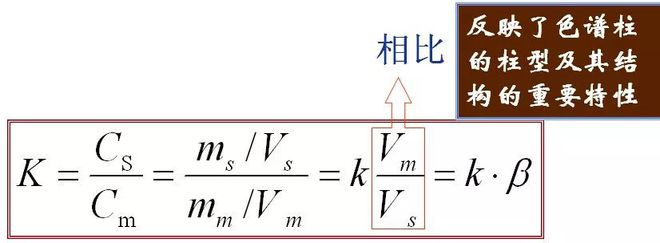
5、Coeficientul de partiție (K) În echilibru, raportul dintre concentrația unei componente în faza (s) staționară și faza mobilă (m), numit coeficient de partiție.Formula este următoarea

Relația dintre K și k:
Reflectă tipul stâlpului și proprietățile sale importante ale structurii nodului
rezumat scurt
Relația dintre valoarea de retenție și factorul de capacitate și coeficientul de partiție:
Separarea cromatografică se bazează pe diferența în capacitatea de adsorbție sau dizolvare a fiecărui component dintr-o probă relativă fixă, care poate fi exprimată cantitativ prin mărimea valorii coeficientului de partiție K (sau factorului de capacitate k).
Componentele cu capacitate puternică de adsorbție sau dizolvare au coeficient de partiție mare (sau factor de capacitate) și timp de retenție lung.În schimb, componentele cu adsorbție sau solubilitate slabă au un coeficient de partiție mic și un timp de retenție scurt.
Teoria de bază a cromatografiei
1. Teoria tăvilor
(1) Propune -- teoria termodinamică
A început cu modelul de placă turn propus de Martin și Synge.
Coloana de fracționare: în tavă de mai multe ori de echilibru gaz-lichid, în funcție de punctul de fierbere al diferitelor separări.
Coloană: Componentele sunt echilibrate prin mai multe partiții între cele două faze și separate în funcție de diferiți coeficienți de partiție.
(2) Ipoteza
(1) Există multe tăvi în coloană, iar componentele pot ajunge rapid la echilibrul de distribuție în intervalul tăvii (adică înălțimea tăvii).
(2) Faza mobilă intră în coloană, nu continuu, ci pulsatorie, adică fiecare trecere este un volum de coloană.
(3) Când proba a fost adăugată la fiecare placă de coloană, difuzia probei de-a lungul axei coloanei ar putea fi neglijată.
(4) Coeficientul de partiție este egal pe toate tăvile, independent de cantitatea de componente.Adică, coeficientul de partiție este constant pe fiecare taban.
(3) Principiu
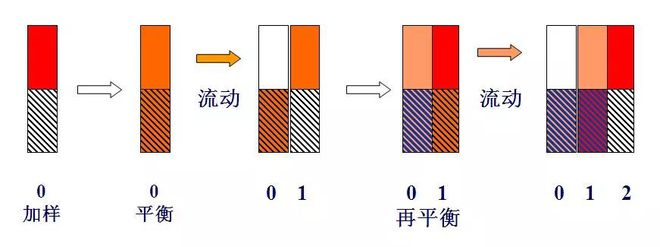
Schema schematică a teoriei tăvilor
Dacă în tava nr. 0 se adaugă o componentă de unitate de masă și anume m=1 (de exemplu, 1mg sau 1μg), iar după echilibrul de distribuție, pentru că k=1 și anume ns=nm, nm=ns=0,5.
Când un volum al plăcii (lΔV) de gaz purtător intră în placa 0 sub formă de pulsație, gazul purtător care conține componenta nm în faza gazoasă este împins pe placa 1. În acest moment, componenta ns din faza lichidă a plăcii 0 iar componenta nm din faza gazoasă a plăcii 1 va fi redistribuită între cele două faze.Prin urmare, cantitatea totală de componente conținute în placa 0 este de 0,5, în care fazele gazoase și lichide sunt fiecare 0,25, iar cantitatea totală conținută în placa 1 este de asemenea 0,5.Fazele gazoase și lichide au fost, de asemenea, 0,25.
Acest proces se repetă de fiecare dată când un nou gaz purtător de volum al plăcii este pulsat în coloană (vezi tabelul de mai jos).
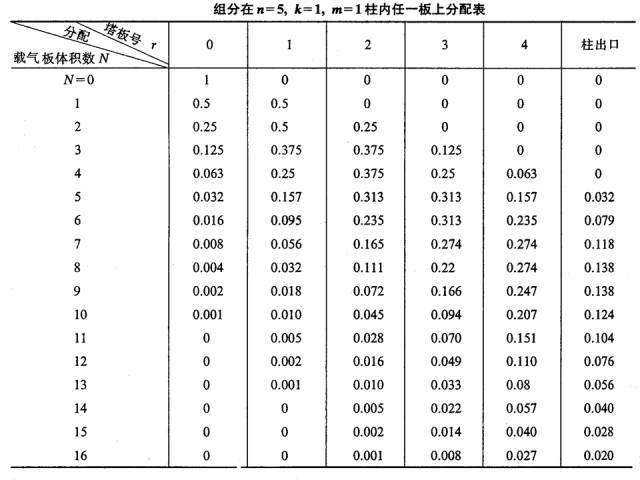
(4) Ecuația curbei cromatografice de scurgere

σ este abaterea standard, este timpul de retenție, C este concentrația în orice moment,
C, este concentrația de injectare, adică cantitatea totală de componente (aria vârfului A).
(5) parametrii de eficiență a coloanei
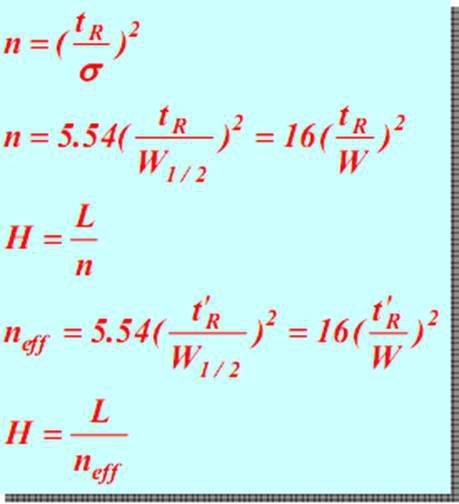
La un tR constant, cu cât W sau w 1/2 este mai mic (adică vârful mai îngust), cu atât este mai mare numărul de plăci teoretice n, cu atât înălțimea teoretică a plăcii este mai mică și eficiența de separare a coloanei este mai mare.Același lucru este valabil și pentru tava de teorie eficientă neff.Prin urmare, numărul teoretic de tăvi este un indice pentru evaluarea eficienței coloanelor.
(5) Caracteristici și deficiențe
> Avantaje
Teoria tăvii este semi-empirică și explică forma curbei de ieșire
Sunt ilustrate procesele de împărțire și separare a componentelor
Se propune un indice pentru evaluarea eficienței coloanei
> Limitări
Componentele nu pot ajunge cu adevărat la echilibrul de distribuție în cele două faze:
Difuzia longitudinală a componentelor în coloană nu poate fi ignorată:
Nu a fost luată în considerare influența diferiților factori cinetici asupra procesului de transfer de masă.
Relația dintre efectul coloanei și viteza de curgere a fazei mobile nu poate fi explicată:
Nu este clar ce factori principali afectează efectul coloanei
Aceste probleme sunt rezolvate satisfăcător în teoria ratei.
2. Teoria ratei
În 1956, savantul olandez VanDeemter et al.a absorbit conceptul de teoria tăvii și a combinat factorii cinetici care afectează înălțimea tăvii, a prezentat teoria cinetică a procesului cromatografic - teoria ratei și a derivat ecuația VanDeemter.Consideră procesul cromatografic ca un proces dinamic de neechilibru și studiază influența factorilor cinetici asupra lărgirii vârfului (adică efectul coloanei).
Mai târziu, Giddings și Snyder și colab.a propus ecuația vitezei cromatografiei lichide (și anume ecuația Giddings) pe baza ecuației VanDeemter (numită mai târziu ecuația vitezei cromatografiei în gaze) și în funcție de diferența de proprietăți dintre lichid și gaz.
(1) Ecuația Van Deemter
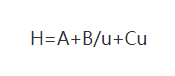
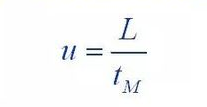
Unde: H: este înălțimea tablei
A: coeficientul termenului de difuzie turbionar
B: coeficientul termenului de difuzie moleculară
C: coeficientul termenului de rezistență de transfer de masă
(2) Ecuația lui Giddings
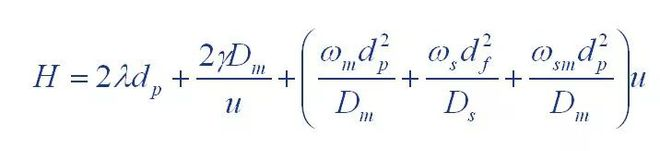
Analiza cantitativa si calitativa
(1) Analiză calitativă
Analiza cromatografică calitativă este de a determina compușii reprezentați de fiecare vârf cromatografic.Deoarece diferite substanțe au valori de retenție definite în anumite condiții cromatografice, valoarea de retenție poate fi utilizată ca indice calitativ.Pe valorile de retenție se bazează în prezent diferite metode calitative cromatografice.
Cu toate acestea, substanțe diferite pot avea valori de retenție similare sau identice în aceleași condiții cromatografice, adică valorile de retenție nu sunt exclusive.Astfel, este dificil să se caracterizeze o probă complet necunoscută doar pe baza valorilor de retenție.Dacă pe baza înțelegerii sursei, naturii și scopului probei, se poate face o judecată preliminară a compoziției probei și se pot utiliza următoarele metode pentru a determina compusul reprezentat de vârful cromatografic.
1. Control calitativ folosind substanțe pure
În anumite condiții cromatografice, o necunoscută are doar un timp de retenție definit.Prin urmare, necunoscutul poate fi identificat calitativ prin compararea timpului de retenție al substanței pure cunoscute în aceleași condiții cromatografice cu timpul de retenție al substanței necunoscute.Dacă cele două sunt la fel, substanța necunoscută poate fi o substanță pură cunoscută;Altfel, necunoscutul nu este substanța pură.
Metoda de control al substanței pure este aplicabilă numai substanței necunoscute a cărei compoziție a fost cunoscută, a cărei compoziție este relativ simplă și a cărei substanță pură este cunoscută.
2. Metoda valorii relative de retenție
Valoarea relativă de retenție α, se referă la ajustarea dintre componenta i și materialele de referință Raportul valorilor de retenție:
Se schimbă doar odată cu schimbarea fixativului și a temperaturii coloanei și nu are nimic de-a face cu alte condiții de funcționare.
La o anumită fază staționară și temperatura coloanei, valorile de retenție ajustate ale componentei i și respectiv substanței de referință s sunt măsurate și apoi calculate conform formulei de mai sus.Valorile relative de retenție obținute pot fi comparate calitativ cu valorile corespunzătoare din literatură.
3, adăugând substanțe cunoscute pentru a crește metoda înălțimii vârfului
Când există multe componente în proba necunoscută, vârfurile cromatografice obținute sunt prea dense pentru a fi identificate cu ușurință prin metoda de mai sus sau când proba necunoscută este utilizată doar pentru analiza articolului specificat.
„Mai întâi se face o cromatogramă a unei probe necunoscute și apoi se obține o altă cromatogramă prin adăugarea unei substanțe cunoscute la proba necunoscută”.Componentele cu înălțimi crescute ale vârfurilor pot fi cunoscute pentru astfel de substanțe.
4. Păstrați metoda calitativă a indicelui
Indicele de retenție reprezintă comportamentul de retenție al substanțelor pe fixative și este în prezent indicele calitativ cel mai utilizat și recunoscut la nivel internațional în GC.Are avantajele unei reproductibilități bune, standard uniform și coeficient de temperatură mic.
Indicele de retenție este legat doar de proprietățile fazei staționare și ale temperaturii coloanei, dar nu și de alte condiții experimentale.Precizia și reproductibilitatea sa sunt excelente.Atâta timp cât temperatura coloanei este aceeași cu cea a fazei staționare, valoarea din literatură poate fi aplicată pentru identificare și nu este necesară utilizarea materialului pur pentru comparație.
(2)Analiza cantitativă
Baza pentru cuantificarea cromatografică:
Sarcina analizei cantitative este de a găsi o sută de componente din proba mixtă
Conținut fracționat.Cuantificarea cromatografică s-a bazat pe următoarele: când condițiile de funcționare au fost consistente, a fost
Masa (sau concentrația) componentei măsurate este determinată de semnalul de răspuns dat de detector
Este proporțională.Și anume:
Baza pentru cuantificarea cromatografică:
Sarcina analizei cantitative este de a găsi o sută de componente din proba mixtă
Conținut fracționat.Cuantificarea cromatografică s-a bazat pe următoarele: când condițiile de funcționare au fost consistente, a fost
Masa (sau concentrația) componentei măsurate este determinată de semnalul de răspuns dat de detector
Este proporțională.Și anume:
1. Metoda de măsurare a zonei de vârf
Zona de vârf este datele cantitative de bază furnizate de cromatograme, iar acuratețea măsurării zonei de vârf afectează direct rezultatele cantitative.Au fost utilizate diferite metode de măsurare pentru vârfurile cromatografice cu diferite forme ale vârfurilor.
Este dificil de găsit valoarea exactă a iernii în analiza cantitativă:
Pe de o parte, din cauza dificultății de a măsura cu precizie volumul absolut de injecție: pe de altă parte
Aria vârfului depinde de condițiile cromatografice, iar banda cromatografică trebuie menținută atunci când valoarea este măsurată.
Nu este nici posibil, nici convenabil să faci același lucru.Și chiar dacă poți înțelege bine
Valoarea exactă, și pentru că nu există un standard unificat și nu poate fi aplicat direct.
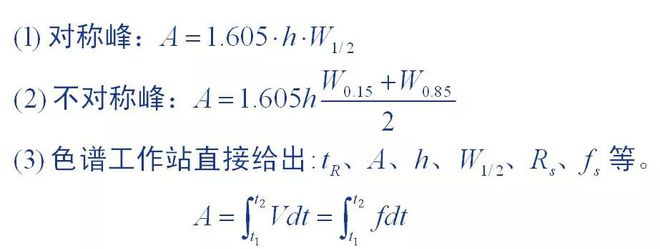
2.Factor de corecție cantitativ
Definiția factorului de corecție cantitativă: cantitatea de componente care intră în detector (m)
Raportul dintre aria sa de vârf cromatografică (A) sau înălțimea vârfului () este o constantă de proporționalitate (,
Constanta de proporționalitate se numește factor de corecție absolut pentru componentă.
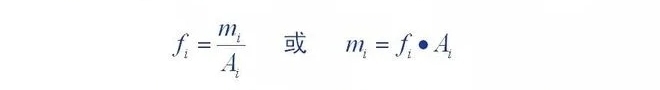
Este dificil de găsit valoarea exactă a iernii în analiza cantitativă:
Pe de o parte, din cauza dificultății de a măsura cu precizie volumul absolut de injecție: pe de altă parte
Aria vârfului depinde de condițiile cromatografice, iar banda cromatografică trebuie menținută atunci când valoarea este măsurată.
Nu este nici posibil, nici convenabil să faci același lucru.Și chiar dacă poți înțelege bine
Valoarea exactă, și pentru că nu există un standard unificat și nu poate fi aplicat direct.
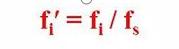
Adică, factorul de corecție relativ al unei componente este componenta și materialul de referință s
Raportul factorilor de corecție absoluti.
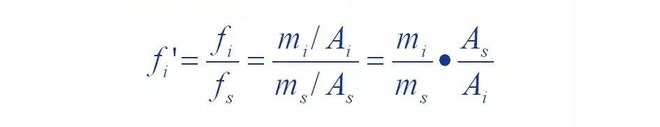
Se poate observa că factorul de corecție relativă este atunci când calitatea componentei față de standard.
Când substanța s este egală, aria vârfului materialului de referință este aria vârfului componentei
Multiplu.Dacă o componentă are masa m și aria vârfului A, atunci numărul de f'A
Valorile sunt egale cu aria vârfului materialului de referință cu masa de.Cu alte cuvinte,
Prin factorul de corecție relativă, zonele de vârf ale fiecărei componente pot fi separate
Convertit în zona de vârf a materialului de referință egală cu masa acestuia, apoi raportul
Standardul este unificat.Deci aceasta este metoda normalizată pentru a afla procentul fiecărei componente
Baza cantității.
Metoda de obținere a factorului de corecție relativă: valorile factorului de corecție relativă au fost comparate doar cu a fi
Masurarea este legata de standard si de tipul de detector, dar de banda de operare
Nu contează.Prin urmare, valorile pot fi preluate din referințele din literatură.Dacă textul
Dacă nu găsiți valoarea dorită în ofertă, o puteți determina și singur.Metoda de determinare
Metodă: O anumită cantitate din substanța măsurată zece material de referință selectat → transformat într-o anumită concentrație
Au fost măsurate zonele de vârf cromatografice A și As ale celor două componente.
Asta e formula.
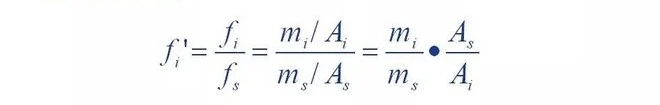
3. Metoda de calcul cantitativ
(1) Metoda normalizării zonei
Suma conținutului tuturor fracțiilor fără vârf a fost calculată ca 100% pentru cuantificare
Metoda se numește normalizare.Formula sa de calcul este următoarea:
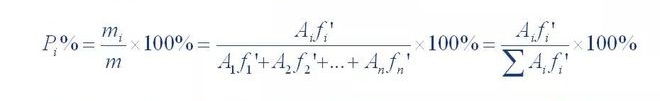
Unde P,% este conținutul procentual al componentelor testate;A1, A2... A n este componenta 1.Aria vârfului de 1~n;f'1, f'2... f'n este factorul de corecție relativ pentru componentele de la 1 la n.
(2) metoda standard extern
Metoda de comparare cantitativă între semnalul de răspuns al componentei care urmează să fie testată în probă și componenta pură care urmează să fie testată ca martor.
(3) Metoda standard intern
Așa-numita metodă standard intern este o metodă în care o anumită cantitate de substanță pură este adăugată la soluția standard a substanței testate și soluția de probă ca standard intern, apoi analizată și determinată.
(3) metoda de adăugare standard
Metoda de adăugare standard, cunoscută și ca metoda de adăugare internă, este adăugarea unei anumite cantități de (△C)
Referința substanței de testat a fost adăugată la soluția de probă care urmează să fie testată și testul a fost adăugat la test
Vârful soluției de probă după substanță a fost mai mare decât cel al soluției de probă inițială
Creșterea ariei (△A) a fost utilizată pentru a calcula concentrația substanței în soluția de probă
Conținut (Cx)
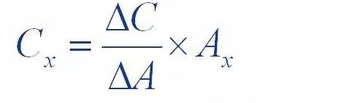
Unde Ax este aria de vârf a substanței care trebuie măsurată în proba originală.

Ora postării: 27-mar-2023